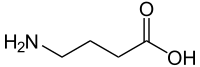
GABA bindet an spezifische biologische Makromoleküle. So aktiviert es ionotrope und metabotrope GABA-Rezeptoren; es passiert Membranen über plasmalemmale (GAT) und vesikuläre (VGAT) Transporter und ist Substrat einer spezifischen Transaminase.
- GABAA-Rezeptoren: Der GABA-Rezeptor vom Typ A ist ein Chlorid-Ionenkanal, der über Liganden gesteuert wird. GABA bindet als orthosterischer Ligand an eine extrazellulär gelegene Domäne des Rezeptors, der als Transmembran-Protein die Zellmembran durchspannt und aus fünf Protein-Untereinheiten zusammengesetzt ist. Diese Bindungsstelle liegt an den Schnittstellen β+/α- der Untereinheiten; die elektrophysiologischen Eigenschaften von GABA sind stark abhängig vom jeweiligen Aufbau des Rezeptortyps.
- Der Bindungskomplex wurde 2018 mittels Elektronenmikroskopie näher charakterisiert. In überwiegend gestreckter Konformation bindet GABA mit seiner Aminogruppe an die Schleifen B und C der Rezeptoruntereinheit beta (β), und zwar über eine Salzbrücke mit Glutaminsäure (β-E155), eine aromatische Kation–Pi-Bindung (β-Y205) und eine Wasserstoffbrückenbindung (β-Y97). Die Carboxygruppe des Liganden geht zwei Wasserstoffbrückenbindungen ein (β-T202 und α-T129) und bildet mit der Rezeptoruntereinheit alpha (α) eine Salzbrücke über Arginin (α-R66). In seiner Lage stabilisiert wird der Ligand durch umgebende Aromaten (β-Y205, β-F200, β-Y157, α-F64). Schwach bindet GABA auch an homologe Bindungsstellen α+/β-. GABA stabilisiert gebunden die geöffnete Konformation des Rezeptors, erhöht damit den Anionen-Einstrom, und führt so zu einer entsprechenden Änderung des Membranpotentials.
- GABAA-ρ-Rezeptoren: Der einst als GABAC-Rezeptor bezeichnete Typ ist ebenfalls ein ionotroper Rezeptor. Er unterscheidet sich vom GABAA-Rezeptor dadurch, dass er aus ρ-Untereinheiten zusammengesetzt ist. An diesem Rezeptor sind pharmakologische Substanzen wie Benzodiazepine und Barbiturate unwirksam.
- GABAB-Rezeptoren: Dieser Typ gehört zu den G-Protein-gekoppelten Rezeptoren (metabotrop). Er vermittelt eine erhöhte Öffnungswahrscheinlichkeit von Kalium-Ionenkanälen. Dies führt zur Hyperpolarisation der Zellmembran. Weiterhin wird die Offenwahrscheinlichkeit für Calcium-Kanäle vermindert. Dieser Effekt macht sich hauptsächlich präsynaptisch bemerkbar, hier wird die Transmitter-Ausschüttung vermindert.