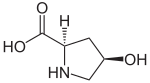
4-Hydroxypyrrolidin-2-carbonsäure existiert in vier Stereoisomeren, in unserer Umwelt spielt nur das (2S,4R)-Isomere als proteinogene Aminosäure eine Rolle. Enantiomer zur natürlichen (2S,4R)-Form ist die (2R,4S)-Form. Die (2S,4S)-Form und die (2R,4R)-Form sind Diastereomere der in Proteinen zu findenden (2S,4R)-4-Hydroxypyrrolidin-2-carbonsäure [Synonym: (2S,4R)-4-Hydroxyprolin].
Wenn in der Literatur und in diesem Artikel von Hydroxyprolin – ohne weitere Zusätze – die Rede ist, ist das natürliche (2S,4R)-Hydroxyprolin [Synonym: L-4-Hydroxyprolin] gemeint. Die anderen drei Isomere sind von geringer Bedeutung.
| Isomere von 4-Hydroxypyrrolidin-2-carbonsäure | ||||
| Name | (2S,4R)-4-Hydroxypyrrolidin-2-carbonsäure | (2R,4S)-4-Hydroxypyrrolidin-2-carbonsäure | (2S,4S)-4-Hydroxypyrrolidin-2-carbonsäure | (2R,4R)-4-Hydroxypyrrolidin-2-carbonsäure |
| Andere Namen | L-4-Hydroxyprolin | trans-4-Hydroxy-D-proline | ||
| Strukturformel |  |
 |
 |
 |
| CAS-Nummer | 51-35-4 | 3398-22-9 | 618-27-9 | 2584-71-6 |
| 6912-67-0 (unspez.) | ||||
| EG-Nummer | 200-091-9 | 625-221-5 | 210-542-1 | 219-963-5 |
| ? (unspez.) | ||||
| ECHA-Infocard | 100.000.084 | 100.153.738 | 100.009.585 | 100.018.149 |
| ? (unspez.) | ||||
| PubChem | 5810 | 440074 | 440015 | 440014 |
| 825 (unspez.) | ||||
| Wikidata | Q12460151 | Q72481402 | Q27103674 | Q27101809 |
| Q411237 (unspez.) | ||||