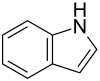
Die Indol-Chemie begann mit dem Studium des häufig verwendeten Farbstoffs Indigo. Indigo kann in Isatin und weiter zu Oxindol umgewandelt werden. 1866 reduzierte Adolf von Baeyer Oxindole mit Hilfe von Zinkstaub zu Indol. 1869 schlug er eine Strukturformel für Indol vor.
Bestimmte Indolderivate waren wichtige Farbstoffe bis zum Ende des 19. Jahrhunderts. In den 1930er-Jahren stieg das Interesse an Indol, als bekannt wurde, dass Indol Grundbestandteil vieler wichtiger Naturstoffe wie Alkaloide (zum Beispiel Strychnin und Auxin) und der Aminosäure Tryptophan und von ihr abgeleiteter Neurotransmitter (Serotonin, Melatonin) ist. Es bleibt ein aktiver Bereich der Forschung bis heute.