Production de viande sans souffrance animale : un système de co-culture basé sur la photosynthèse
Des chercheurs créent une alternative durable au sérum pour la viande cultivée
Annonces
Il existe un besoin pressant de technologies de production de viande respectueuses de l'environnement pour répondre à la demande alimentaire mondiale croissante. La production de viande cultivée est l'une de ces technologies qui attire beaucoup d'attention en tant qu'alternative à la production de viande conventionnelle. Développée pour la première fois en 2012, la viande cultivée est simplement produite en cultivant des cellules musculaires d'animaux en laboratoire.
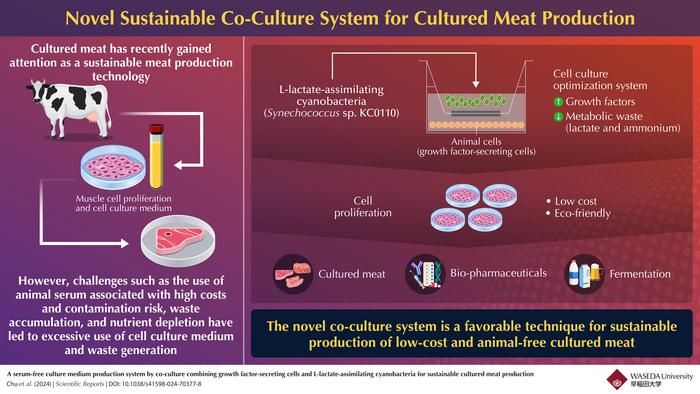
Des chercheurs ont mis au point un système dans lequel des cellules hépatiques et des micro-organismes photosynthétiques peuvent être cultivés ensemble pour créer un milieu peu coûteux et respectueux de l'environnement permettant de cultiver des cellules musculaires sans utiliser de sérum animal.
Dr. Tatsuya Shimizu from Tokyo Women’s Medical University, Japan
Généralement, la production de viande cultivée nécessite du sérum (ou la partie liquide du sang) provenant des animaux, qui est essentiel pour la croissance des cellules musculaires dans le milieu de culture, car le sérum contient des protéines abondantes qui favorisent la croissance des cellules musculaires. L'utilisation de sérum animal pose des problèmes importants pour de multiples raisons telles que les coûts élevés, le risque de contamination et les préoccupations éthiques. Il est donc nécessaire de mettre au point des méthodes de culture qui permettent aux cellules musculaires de se développer sans utiliser de sérum.
Une équipe de recherche dirigée par le professeur Tatsuya Shimizu de la Tokyo Women's Medical University, avec l'étudiant en doctorat Shanga Chu et le professeur Toru Asahi de la Waseda University, le professeur Yuji Haraguchi de la Tokyo Women's Medical University et le professeur Tomohisa Hasunuma de la Kobe University, a mis au point un nouveau système de culture de cellules musculaires sans sérum à l'aide de micro-organismes photosynthétiques. Leurs résultats ont été publiés dans Scientific Reports le 23 août 2024.
Normalement, le sérum animal fournit des protéines appelées facteurs de croissance qui sont essentielles à la croissance des cellules musculaires. Toutefois, les cellules hépatiques de rat sont également connues pour sécréter ces facteurs de croissance. Les chercheurs ont découvert que le milieu restant après la culture de ces cellules hépatiques (ou le surnageant) contient des facteurs de croissance et peut soutenir la croissance des cellules musculaires sans utiliser de sérum. "Bien qu'un plus grand nombre de cellules sécrétant des facteurs de croissance et une culture plus longue produisent une plus grande quantité de facteurs de croissance, l'inconvénient est que les cellules produisent également des déchets comme le lactate et l'ammoniaque dans le milieu en même temps, ce qui finit par entraver la croissance des cellules musculaires", explique Shimizu.
L'élimination des déchets est donc cruciale pour améliorer les performances de ce surnageant de culture en tant qu'alternative au sérum animal. Pour résoudre ce problème, les chercheurs ont développé des cyanobactéries assimilatrices de L-lactate (micro-organismes photosynthétiques) dotées de gènes de conversion du lactate en pyruvate, capables d'absorber des métabolites de déchets nocifs, tels que le lactate et l'ammoniac, et de les convertir en nutriments pour les cellules animales (cellules hépatiques de rat et cellules musculaires), tels que le pyruvate et les acides aminés.
Dans cette étude, le groupe de recherche a proposé un nouveau système dans lequel les cellules hépatiques de rat sécrétant des facteurs de croissance seraient cocultivées ou cultivées avec les cyanobactéries modifiées, et le surnageant de cette coculture pourrait alors être utilisé pour promouvoir la croissance des cellules musculaires sans sérum. Les chercheurs ont constaté que la coculture de cyanobactéries avec des cellules de foie de rat permettait une réduction de 30 % du lactate et de plus de 90 % de l'ammoniaque. En outre, les nutriments produits par les cyanobactéries ont permis de réduire l'épuisement des nutriments par les cellules hépatiques de rat, ce qui s'est traduit par une abondance de nutriments tels que le glucose et le pyruvate dans le surnageant de co-culture par rapport au surnageant recueilli lorsque les cellules hépatiques de rat étaient cultivées seules.
Lorsque ce surnageant de coculture a été utilisé pour cultiver des cellules musculaires, les chercheurs ont constaté que le taux de croissance des cellules musculaires était trois fois plus élevé que celui observé lorsque seules des cellules de foie de rat étaient utilisées. Cela démontre que la coculture de cyanobactéries améliore considérablement les performances du surnageant de culture en tant qu'alternative au sérum et optimise la culture cellulaire grâce au recyclage des déchets.
"Notre étude fournit un nouveau système de culture cellulaire durable et peu onéreux, avec une large applicabilité dans divers domaines impliquant l'agriculture cellulaire, tels que la production de viande cultivée, la fermentation, la production biopharmaceutique et la médecine régénérative. En outre, en tant que technologie permettant de produire de la viande sans tuer d'animaux, la culture de cellules animales avec des micro-organismes photosynthétiques pourrait contribuer à répondre non seulement aux défis futurs en matière de sécurité alimentaire, mais aussi aux préoccupations éthiques et aux questions liées au changement climatique", conclut M. Shimizu.
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Anglais peut être trouvé ici.





































